Zāļu valsts aģentūra (ZVA) 2015. gadā, vērtējot zāļu dokumentāciju saistībā ar kvalitāti, drošumu un efektivitāti, veikusi vairāk nekā 2000 ekspertīžu zāļu dokumentācijas vispārējai, ķīmiskai un farmaceitiskai, kā arī preklīniskai un klīniskai daļai, liecina ZVA 2015. gada publiskajā pārskatā paustā informācija.
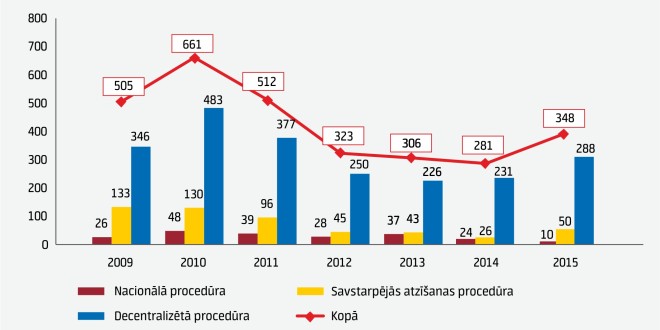
2015. gadā par 57 zālēm tika sagatavoti novērtējuma ziņojumi ZVA Zāļu reģistrācijas komisijai lēmuma pieņemšanai par zāļu reģistrāciju un pārreģistrāciju nacionālajā procedūrā. Latvija kā atsauces valsts 2015. gadā veiksmīgi novadījusi vienu savstarpējās atzīšanas procedūru (mutual recognition procedure – MRP) un četras decentralizētās procedūras (decentralised procedure – DCP), kā arī piecas MRP pārreģistrācijas procedūras. ZVA pērn no citām dalībvalstīm pārņēma četras DCP procedūras, kurās kļuva par atsauces valsti. Kā atsauces valsts Latvija 2015. gadā uzsāka piecas DCP procedūras un divas MRP pārreģistrācijas procedūras.
Kopā 2015. gada laikā ZVA veiktas 338 MRP/DCP reģistrācijas procedūras un 231 pārreģistrācijas procedūra.
2015. gadā tika iesniegtas un vērtētas 9819 reģistrētu zāļu dokumentācijas izmaiņas. Pārskata gadā saņemts 31 pieteikums vērtēt produkta atbilstību zāļu definīcijai, par kuriem ZVA ir sniegusi atzinumus par produktu statusu. 2015. gadā tika vērtēti 138 periodiski atjaunojamie drošuma ziņojumi. 2015. gadā publicēti 13 publiskie vērtējuma ziņojumi nacionālā procedūrā reģistrētām zālēm, kas saskaņoti ar reģistrācijas īpašniekiem.
Recepšu un bezrecepšu zāļu īpatsvars Latvijas Zāļu reģistrā gadu no gada līdzīgs – aptuveni 80% ir recepšu zāles, un 20% bezrecepšu zāles. Tomēr 2015. gadā šī attiecība bija 82% un 18%.
www.farmacija-mic.lv

 Medikamentu Informācijas Centrs Farmācijas portāls | Viss par farmāciju
Medikamentu Informācijas Centrs Farmācijas portāls | Viss par farmāciju