Vulvovaginālā kandidoze (VVK), ko galvenokārt izraisa Candida albicans, ir izplatīta maksts infekcija, kura vismaz vienu reizi dzīves laikā skar līdz 75% sieviešu reproduktīvā vecumā. Nereti VVK vairākkārt atkārtojas, radot recidivējošu vulvovaginālu kandidozi (RVVK). Pacienšu izglītošana un atbilstoša pretsēnīšu līdzekļu izvēle var novērst RVVK attīstību, kā arī mazināt rezistences iespēju.
Candida, sēnīte no askusēņu (Ascomycota) nodalījuma, kolonizē elpceļus, uroģenitālo, kuņģa un zarnu traktu vairāk nekā 30% cilvēku viņu mūža laikā (1).
Candida sugas ir izplatītākās maksts mikrobioma sēnītes un var izraisīt maksts infekciju. VVK galvenokārt izraisa Candida albicans. Citas sugas, kas arī izraisa VVK, ir C. glabrata, C. krusei, C. parapsilosis, C. africana un C. tropicalis.
Ja gada laikā ir vairāk nekā trīs VVK epizodes, tā ir RVVK, kas skar aptuveni 9% sieviešu. RVVK parasti skaidro ar nepietiekamu organisma aizsargspēju pret Candida kolonizāciju, taču jaunākie pētījumi liek domāt par pārmērīgu lokālu imūnsistēmas reakciju gļotādā, nevis par vāju sievietes organisma aizsargspēju (1).
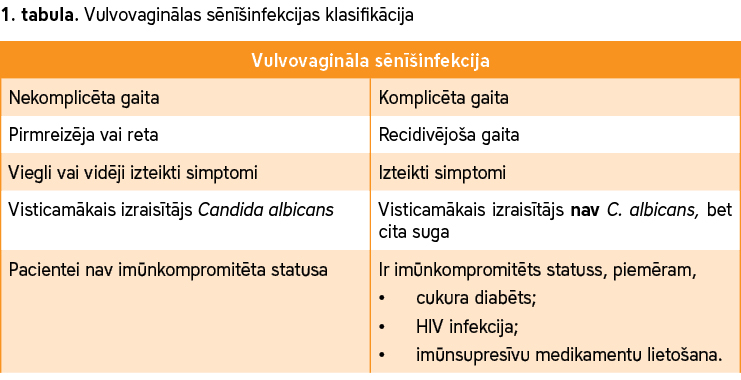
Būtiski noteikt, vai VVK ir pirmreizēja/reta, viegli padodas ārstēšanai, vai arī tās gaita ir komplicēta, infekcija atgriežas un tā ir RVVK (sk. 1. tabulu).
Visbiežāk sastopamās VVK pazīmes un simptomi ir izdalījumi no maksts, vulvas nieze, dedzinoša sajūta un sāpes urinējot. Simptomātiska VVK saistīta ar paaugstinātu maksts polimorfonukleāro neitrofilo leikocītu (PMN) infiltrāciju un sēnīšu koncentrāciju, kas liecina, ka VVK simptomus mediē PMN (1).
Faktori, kas pacientēm ar RVVK var mainīt normālu maksts mikrobiomu un izraisīt Candida sēnīšinfekcijas uzliesmojumu, ir mainīts ūdeņraža peroksīdu producējošā Lactobacillus līdzsvars un paaugstināts estrogēna līmenis.
VVK biežāk ir sievietēm reproduktīvā vecumā, izplatībai palielinoties līdz ar vecumu līdz menopauzei. Pēc menopauzes VVK vairs nav bieži sastopama, ja vien sieviete nelieto estrogēnus. Infekcija nav izplatīta pirmspubertātes vecumā.
Diagnostikā lielākā nozīmē ir klīniskai ainai un tipiskai atradei ginekoloģiskās apskates laikā. Apstiprināšanai izmanto maksts iztriepes mikroskopiju, lai identificētu rauga sēnītes un to hifas:
- natīva – ārsta kabinetā, izmantojot sāls šķīdumu un 10% kālija hidroksīdu;
- fiksēta – laboratorijas apstākļos ar Grama krāsojumu.
Komplicētas, recidivējošas infekcijas gadījumā, kā arī tad, ja vulvovagināla sēnīšinfekcija nepakļaujas ārstēšanai, veic uzsējumu no maksts.
Jāņem vērā, ka precīzai diagnostikai ir liela nozīme, jo tikai 28% sieviešu pēc simptomiem nosaka sev pareizu VVK diagnozi, 53% gadījumu pacientēm simptomus bija radījusi bakteriāla vaginoze, retāk – trihomonoze, gonoreja vai hlamidioze. Tikai 34% sieviešu bijusi izolēta vulvovagināla sēnīšinfekcija bez citiem iespējamiem vaginālas infekcijas izraisītājiem. Šie fakti liek secināt, ka sievietēm būtiski vērsties pie ārsta, ja simptomi nemazinās pēc viena lokālas terapijas kursa (2).
VVK riska faktori
VVK riska faktori ir 2. tipa cukura diabēts, antibiotikterapija, imūnsupresantu, kortikoīdu, intrauterīnas spirāles, kā arī citu hormonālu kontracepcijas līdzekļu lietošana. Lielāks RVVK risks ir eiropeīdām, brazīliešu, ēģiptiešu, ķīniešu un afroamerikāņu izcelsmes sievietēm (1).
Ārstēšana
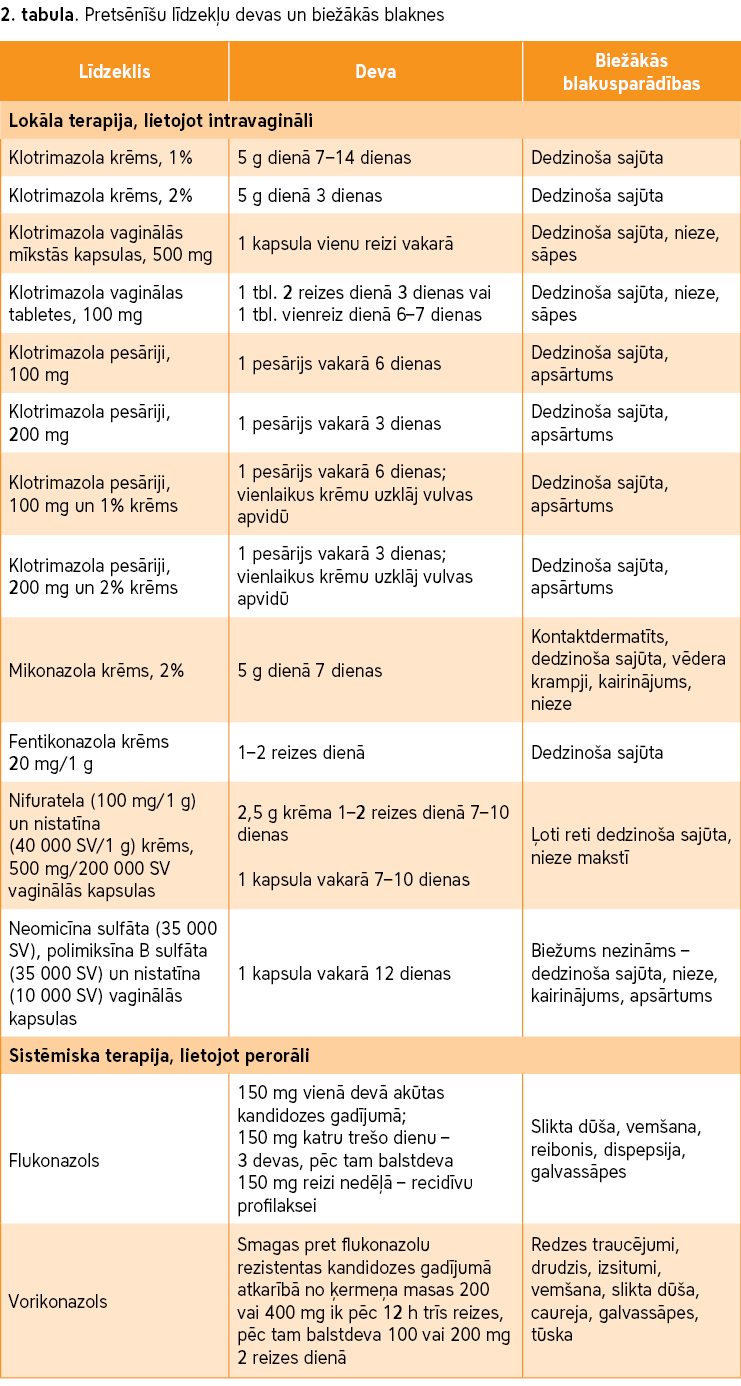
VVK var ārstēt ar lokāliem vai perorāliem pretsēnīšu līdzekļiem, visbiežāk azoliem, taču šīs zāles nenovērš atkārtotu infekciju. Dažos gadījumos pacientēm var būt nepieciešami profilaktiski pretsēnīšu līdzekļi (1). Nekomplicēta VVK jāārstē ar lokāliem pretsēnīšu līdzekļiem, kuri ir ar līdzvērtīgu efektivitāti. Lokālie pretsēnīšu līdzekļi ir klotrimazola krēms (1%, 2%), pesāriji (100 un 200 mg), mīkstās kapsulas (500 mg), vaginālās tabletes (100 mg), mikonazola gels (2%), fentikonazola krēms u.c.
Maksts mikrobiomu apdzīvo labvēlīgas Lactobacillus ģints baktērijas un raugi. Tādēļ papildus lokāli vai iekšķīgi var izmantot probiotikas, kas satur pienskābās baktērijas, lai līdzsvarotu normālo mikrofloru, kam ir būtiska nozīme VVK gadījumā.

Kā alternatīvu lokālām zālēm nekomplicētas VVK ārstēšanā var iekšķīgi lietot vienu 150 mg flukonazola devu (3). Smagas akūtas VVK gadījumā perorāli lieto 150 mg flukonazola ik pēc 72 stundām, kopā 2–3 devas. C. glabrata vulvovaginīts, kas nereaģē uz perorāliem azoliem (piemēram, flukonazolu), jāārstē ar nistatīna intravagināliem supozitorijiem – 100 000 SV dienā 14 dienas. RVVK ārstē perorāli ar flukonazolu – 150 mg 10–14 dienas; pēc tam 150 mg reizi nedēļā 6 mēnešus (3).
VVK profilakses pasākumi: izvairīties no maksts skalošanas, vulvas mazgāšanas ar ziepēm un citiem higiēnas līdzekļiem. Pacientes jāmudina valkāt kokvilnas apakšveļu, apslaucīties no priekšpuses uz aizmuguri un bieži mainīt higiēniskās paketes vai tamponus menstruāciju laikā.
Retrospektīvā pārskatā par sievietēm pirmsmenopauzes periodā, kurām bija C. albicans izraisīta RVVK, vērtēja ilgtermiņa flukonazola lietošanu (pēc sākotnēja 6 mēnešu flukonazola kursa). Biežākais papildu flukonazola terapijas iemesls bija VVK recidīvs (55,1%), un vidējais flukonazola balstterapijas ilgums bija vairāk nekā 3 gadi. Rezistence pret flukonazolu radās 7,5% pacienšu, kas pabeidza 6 mēnešu terapiju. Novērošanas laikā 93,6% pacienšu (n=51) ziņoja par ieguvumu balstterapijas laikā, taču 80,9% pacienšuu radās recidīvs pēc flukonazola terapijas pārtraukšanas. Šajā pētījumā flukonazola terapija bija efektīva VVK simptomu novēršanai, taču reti pilnīgi atbrīvoja no infekcijas, pēc balstterapijas pārtraukšanas bieži radās VVK recidīvs (5).
2022. gadā ASV Pārtikas un zāļu pārvalde (FDA) RVVK ārstēšanai apstiprinājusi otezekonazolu, kas Eiropā nav reģistrēts. Šis pretsēnīšu līdzeklis indicēts sievietēm bez reproduktīva potenciāla, kuras cieš no RVVK.
Pret vairumu Candida sugu sēnīšu otezekonazols ir vidēji 40 reizes spēcīgāks nekā flukonazols. Otezekonazols ir arī spēcīgs dermatofītu, tostarp Trichophyton rubrum un Trichophyton mentagrophytes, inhibitors (6). Tas lietojams iekšķīgi monoterapijā vai kombinācijā ar flukonazolu.
Biežākās otezekonazola nevēlamās blaknes ir galvassāpes un slikta dūša. Šo līdzekli neiesaka pacientēm ar vidēji smagiem vai smagiem (B vai C klase pēc Child-Pugh) aknu darbības traucējumiem, ar glomerulu filtrācijas ātrumu 15–29 ml/min vai nieru slimību terminālā stadijā. Otezekonazols ir kontrindicēts sievietēm ar reproduktīvo potenciālu, grūtniecēm un sievietēm zīdīšanas periodā, kā arī pacientēm ar paaugstinātu jutību pret otezekonazolu (6).
Farmaceita loma
Farmaceitiem ir izšķiroša loma pacientu situācijas novērtēšanā un ārstēšanas ieteikumu sniegšanā. Novērtējot VVK vai RVVK, jānoskaidro maksts infekciju biežums anamnēzē un iepriekš lietotie medikamenti. Farmaceiti ievāc informāciju, lai noteiktu, vai piemērotas bezrecepšu zāles, vai ārstam jāizvēlas recepšu medikaments. Pacientēm, kam simptomi atkārtojas mazāk nekā 2 mēnešus pēc bezrecepšu zāļu lietošanas, vai sievietēm, kam simptomi neizzūd pēc VVK ārstēšanas ar bezrecepšu zālēm, jākonsultējas ar ārstu par recepšu zāļu izvēli.
Farmaceitiskā konsultācijā jājautā, vai pacientēm, kas lieto perorālos pretsēnīšu līdzekļus, nav iestājusies grūtniecība, jo šo līdzekļu lietošana var kaitēt auglim. Turklāt farmaceitiem jācenšas brīdināt pacientes, kas lieto pretsēnīšu krēmu vai vaginālos supozitorijus, ka tie var bojāt lateksa prezervatīvus un diafragmas, iesakot pacientēm atturēties no dzimumdzīves vai izmantot citas kontracepcijas metodes. Atšķirībā no citām maksts infekcijām VVK vai RVVK gadījumā pacienšu seksuālie partneri nav jāārstē.
Jāatceras, ka perorāli pretsēnīšu līdzekļi mijiedarbojas ar kalcija kanāla blokatoriem, varfarīnu, ciklosporīnu, perorāliem pretdiabēta līdzekļiem, teofilīnu, rifampīnu u.c.
Sagatavojusi Dace Vēja pēc Scurka E., Henault B., Ostroff M. L., Ostroff J. L. Addressing recurrent vulvovaginal candidiasis. US Pharm., 2022; 47 (9): 22–26.
Vēres
- Rosati D., Bruno M., Jaeger M. et al. Recurrent vulvovaginal candidiasis: an immunological perspective. Microorganisms. 2020; 8 (2): 144.
- Ferris D. G., Nyirjesy P., Sobel J. D. et al. Over-the-counter antifungal drug misuse associated with patient-diagnosed vulvovaginal candidiasis. Obstet. Gynecol., 2002; 99: 419–425.
- Pappas P. G., Kauffman C. A., Andes D. R. et al. Clinical practice guideline for the management of candidiasis: 2016 update by the Infectious Diseases Society of America. Clin Infect Dis. 2016; 62 (4): e1–e50.
- CDC. Sexually transmitted infections treatment guidelines, 2021: vulvovaginal candidiasis (VVC). www.cdc.gov/std/treatment-guidelines/candidiasis.htm.
Collins L. M., Moore R., Sobel J. D. Prognosis and long-term outcome of women with idiopathic recurrent vulvovaginal candidiasis caused by Candida albicans. J Low Genit Tract Dis. 2020; 24 (1): 48–52. - Sobel J. D., Nyirjesy P. Oteseconazole: an advance in treatment of recurrent vulvovaginal candidiasis. Future Microbiol. 2021; 16 (18): 1453–1461.
- Scurka E., Henault B., Ostroff M. L., Ostroff J. L. Addressing recurrent vulvovaginla candidiasis. US Pharm., 2022; 47 (9): 22–26.

 Medikamentu Informācijas Centrs Farmācijas portāls | Viss par farmāciju
Medikamentu Informācijas Centrs Farmācijas portāls | Viss par farmāciju