Kopš pērnā gada 28. decembra, kad Latvijā uzsāka vakcināciju pret koronavīrusu, līdz šī gada 12. janvārim Zāļu valsts aģentūrā (ZVA) saņemtie ziņojumi par Covid-19 vakcīnu blaknēm liecina, ka lielākā daļa novēroto blakņu ir zināmas, proti, paredzētas un norādītas vakcīnas lietošanas instrukcijā un zāļu aprakstā. Līdz ar to paredzams, ka šādas blaknes ir iespējamas dažiem cilvēkiem pēc vakcinācijas, norāda ZVA. Kopumā ... Lasīt tālāk »
Medikamenti
EZA palielina devu skaitu, kas iegūstams no “Pfizer/BioNTech” vakcīnas pudelītes
Eiropas Zāļu aģentūra (EZA) izdevusi “Pfizer”-“BioNTech” Covid-19 vakcīnas lietošanas vadlīniju jaunu versiju, ļaujot vienu vakcīnas pudelīti izmantot sešām devām, nevis piecām, kā tas bija līdz šim. Izmantojot specifiskas šļirces, kas paredzētas vakcinēšanai ar vakcīnu “Comirnaty” – pirmo, kas apstiprināta izmantošanai Eiropas Savienībā (ES) -, var droši no pudelītes iegūt vienu papildu devu, paziņojumā norādīja EZA. Izmaiņas vadlīnijās nozīmē, ka laikā, ... Lasīt tālāk »
“CureVac” Covid-19 vakcīnas izstrādē apvieno spēkus ar “Bayer”
Vācijas biotehnoloģiju uzņēmums “CureVac”, kas būtiski pavirzījies uz priekšu Covid-19 vakcīnas izveidē, apvieno spēkus ar Vācijas farmācijas gigantu “Bayer”, lai tas palīdzētu vakcīnas izstrādē un izplatīšanā. “CureVac” pagājušajā mēnesī paziņoja, ka trešās pētījumu fāzes pirmie rezultāti potenciālajai vakcīnai pret jauno koronavīrusu gaidāmi līdz marta beigām. Uzņēmuma izstrādātajā vakcīnā tiek izmantota jaunā tehnoloģija, kas balstīta uz RNS signālmolekulu (mRNA). “CureVac” un ... Lasīt tālāk »
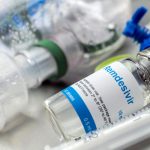
Mainīta medikamenta “Remdesivir” glabāšanas kārtība
30. decembrī Valsts operatīvā medicīniskā komisija (VOMK) lēma mainīt medikamenta “Remdesivir” uzglabāšanas kārtību, kā arī noteica prasības vakcinācijas kabinetu izveidei slimnīcās. Vienlaikus pieņemts arī lēmums, ka vēl līdz 10. janvārim iedzīvotājiem Covid-19 analīzes būs iespējams nodot arī bez ārsta nosūtījuma, ja ir parādījušies slimības simptomi. Šobrīd medikamentu “Remdesivir” uzglabā Rīgas Austrumu klīniskajā universitātes slimnīcā, un nepieciešamības gadījumā pēc ārstu konsīlija ... Lasīt tālāk »
ZVA aicina uzticamu informāciju par Covid-19 vakcīnām meklēt aģentūras mājaslapā
Lai iedzīvotāji varētu ērtāk rast uzticamu un zinātnē balstītu informāciju par vakcīnu pret Covid-19 izstrādi, Zāļu valsts aģentūras (ZVA) tīmekļvietnes sadaļā “Covid-19 ziņas” regulāri tiek aktualizēta un publicēta jaunākā informācija par vakcīnu izstrādes un apstiprināšanas procesu, tai skaitā fakti par vakcīnām. Savukārt informācija par vakcinācijas norisi Latvijā ir pieejama Slimību profilakses un kontroles centra tīmekļvietnes sadaļā “Vakcīnas pret Covid-19”. Tīmekļvietnēs publicēta aktuālā informācija par vakcīnu ... Lasīt tālāk »
Eiropas zāļu aģentūra: “Pfizer” un “BioNTech” vakcīna nesatur vīrusu un nevar izraisīt saslimšanu ar Covid-19
Eiropas Zāļu aģentūras (EZA) un Eiropas Komisijas apstiprinātā farmācijas uzņēmumu “Pfizer” un “BioNTech” izstrādātā vakcīna pret Covid-19, kurai dots nosaukums “Comirnaty”, nesatur pašu vīrusu un nevar izraisīt saslimšanu ar Covid-19, liecina EZA publicētā informācija. Farmācijas uzņēmumu “Pfizer” un “BioNTech” ražotā vakcīna ir paredzēta cilvēkiem vecumā no 16 gadiem un jāsaņem divās injekcijās – tās tiek veiktas rokā ar vismaz 21 ... Lasīt tālāk »
Neapmierinošo rezultātu dēļ “Sanofi” un GSK Covid-19 vakcīnu izstrāde kavēsies
Francijas farmācijas uzņēmums “Sanofi” un Lielbritānijas firma “GlaxoSmithKline” (GSK) piektdien paziņoja, ka to vakcīna pret Covid-19 nebūs gatava izplatīšanai līdz 2021.gada beigām. Eksperimentālās Covid-19 vakcīnas augstākā līmeņa izmēģinājumi atlikti, jo vakcīna nav spējusi radīt pietiekami spēcīgu reakciju gados vecākos cilvēkos. Partneri februārī sāks jaunus otrās fāzes pētījumus ar koncentrētāku antigēnu, jo patlabanējā koncentrācija nav radījusi labu imūno atbildi 50 gadus ... Lasīt tālāk »
ZVA informē par gripas vakcīnu pieejamību
Zāļu valsts aģentūra (ZVA) informē, ka saskaņā ar zāļu lieltirgotavas AS “Recipe Plus” sniegtajiem datiem Latvijas aptiekām un ārstniecības iestādēm 2020. gada 8. decembrī ir piegādāti 2767 iepakojumi pretgripas vakcīnu “Influvac Tetra suspensija injekcijām pilnšļircē”. Pretgripas vakcīnas piegādātas šādām aptiekām un ārstniecības iestādēm – pieejams šeit (Excel). ZVA atgādina, ka vakcīnu skaits katru dienu ir mainīgs un pacienti zāles var iegādāties aptiekās, konsultējoties ... Lasīt tālāk »
Spēkā stāsies grozījumi regulās par narkotisko vielu prekursoriem
Zāļu valsts aģentūra (ZVA) informē, ka 2020. gada 13. decembrī stājas spēkā KOMISIJAS 2020. gada 14. jūlija DELEĢĒTĀ REGULA (ES) 2020/1737, ar ko attiecībā uz konkrētu narkotisko vielu prekursoru iekļaušanu klasificēto vielu sarakstā groza Eiropas Parlamenta un Padomes Regulu (EK) Nr. 273/2004 un Padomes Regulu (EK) Nr. 111/2005 (turpmāk – Regula 2020/1737). Saskaņā ar Regulā 2020/1737 noteikto tiek papildināts 2004. ... Lasīt tālāk »
Lielbritānija sāk iedzīvotāju vakcinēšanu pret Covid-19
Lielbritānijas Nacionālais veselības dienests otrdien, 8. decembrī, sāk programmu iedzīvotāju vakcinēšanai pret jauno koronavīrusu. Aptuveni 70 slimnīcās visā Lielbritānijā cilvēkiem, kas vecāki par 80 gadiem, un veselības aprūpes darbiniekiem tiks injicēta ASV zāļu ražotāja “Pfizer” un Vācijas uzņēmuma “BioNTech” izstrādātā vakcīna pret jauno koronavīrusu. Lielbritānija ir pirmā valsts pasaulē, kas izmantos šo vakcīnu, ko Lielbritānijas zāļu aģentūra apstiprināja pagājušajā nedēļā. ... Lasīt tālāk »

 Medikamentu Informācijas Centrs Farmācijas portāls | Viss par farmāciju
Medikamentu Informācijas Centrs Farmācijas portāls | Viss par farmāciju